CzeekV 使い方 日付について
-
FAERSの場合
FAERSの症例レポートには日付に関するものが複数記載されています。
・有害事象発生日(event_dt)
・製薬会社への報告日(mfr_dt)
・FDAへの報告日(最初にFDAが受理した日)(init_fda_dt)
・FDAへの報告日(直近での受理日)(fda_dt)
・報告送付日(rept_dt)
※()の中身はFAERSのデータ項目名です。の5種類がデモテーブルに含まれています。
また、Therapyテーブルには
・薬剤投与開始日
・薬剤投与終了日
もあります。有害事象に関しては、一つひとつの有害事象に日付があるのではなく、
症例レポート一つに対して報告日なる日付が複数つけられています。
(JADERと大きく違う箇所の一つです)FDAの有害事象自発報告システムは自発報告用の窓口を広く設けていることもあり、
報告機関・報告者によって記載可否の情報があり、各項目の役割が変わってきます。患者の訴えを聴いた医師がすぐ製薬会社やFDAへ有害事象として報告するとも限らないうえ、
医療機関からの報告を受け取った製薬企業も必要な情報をヒアリング、整理してからFDAへの期限内報告を実施します。
その過程で正確な情報、日付を把握できるのは立場によって様々です。ご存知の通りFAERSデータの記載に関する曖昧さは確かに存在しますが、
それらをカバーするための情報も同時に準備されていることがわかります。・JADERでは各薬剤の投与開始日と各有害事象の発現日が記載されている
・FAERSでは各薬剤の投与開始日はあるが1症例1つの有害事象発現日しかない(上記発現日)
これらを理由に、併用薬が存在する場合に有害事象毎の正確な発現時期算出が難しいため発現時期解析はJADAERのほうが適する、
という研究報告もあります。
その報では、ある薬剤を例として有害事象発現日算出に必要なデータ欠損割合もJADERに比較して
FAERSのほうが悪いデータであることも同時に示されています。
この欠損割合が上記のどの日付を対象として計算されたのかが不明であるため何ともいえませんが、
発現時期プロファイリングにはFAERS、JADERともに期待できるところや、反面、注意しなければならないことが多くあることも分かるかと思います。ちなみにCzeekVでは「レポート詳細情報」画面にこれら日付に関する情報を含めています。
(レポート一覧の識別番号をクリックすると表示されます)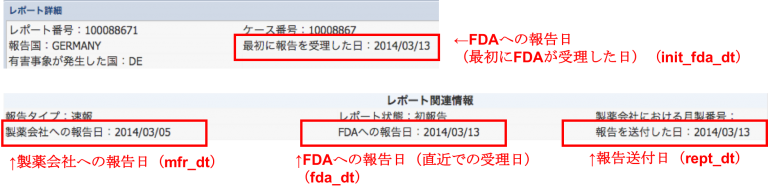
init_fda_dt(最初にFDAが受理した日)は2012年Q4版から追加された項目です。
fda_dtは1997年Q4期の時点から存在します。このことから記載されているボリュームに差があることも理解できるかと思います。また、右図のように「有害事象発生日」も記載が必ずしもあるとは限りません。
(CzeekVでは「副作用発生日時」と表示されています)
レポート一覧に表示されていますので一度確認してみてください。
JADERの場合
一方JADERの場合は、症例報告レポート内の一つひとつの有害事象に発現日が情報として付与されています。
ただし、上記の通りこちらも必ず記載があるとは限りません。
また、日付が異なる場合、薬に関する情報(リチャレンジ、デチャレンジ等)をチェックすることも必要かと思います。
何が原因でその有害事象が発生し報告されているのか等を確認し、交絡因子の調整に役立てます。有害事象発生日の活用について
このように色々ある”日付”を解析対象とした研究報告例もいくつかあります。
「薬剤投与日」から「有害事象発現日」「報告日」までの期間を計算して(引いて1足す等)
薬剤曝露期間と位置づけ、有害事象発生に関する解析をしています。
どの日付を利用するのが適切かはケースによって変わります。
各有害事象に発現日がついていることと抜けデータが少ないことから
期間を設定した解析はJADERが好まれて利用されているケースが多いです。個人的には薬剤の発売日からの報告数の推移や、マスコミ報道後の報告数推移など、
”日付””期間”を見る視点は多くあるかと思っています。バイアス除去にも役立ちそうです。こうした”期間”を見ることで薬理作用・薬物動態を考慮した薬の特徴とあわせて
さらに踏み込んだ研究報告が増えてきていることは興味深いです。その際にデータの特徴と構成を考慮して注意すべき箇所を加味して精度の高い解析を
行うことが重要かと思います。まとめ
・FAERS/JADERそれぞれで日付の種類・内容が異なるので
詳細を理解してから解析を進める。
・”期間”を計算して詳細に解析する場合は、症例レポート記載の他薬剤についても注意する -
お問合わせ
メルマガ登録




